珈创生物 —— 生物技术服务与研发为一体的高新技术企业
优质高效透明
High quality, efficient and transparent
发布时间:2022-06-01 21:35 信息来源: 阅读次数: 次
本文解读的是:《生物制品生产检定用动物细胞基质制备及质量控制》中华人民共和国药典,2020年版,三部,生物制品通则-下。
对生产用细胞基质总的要求
下
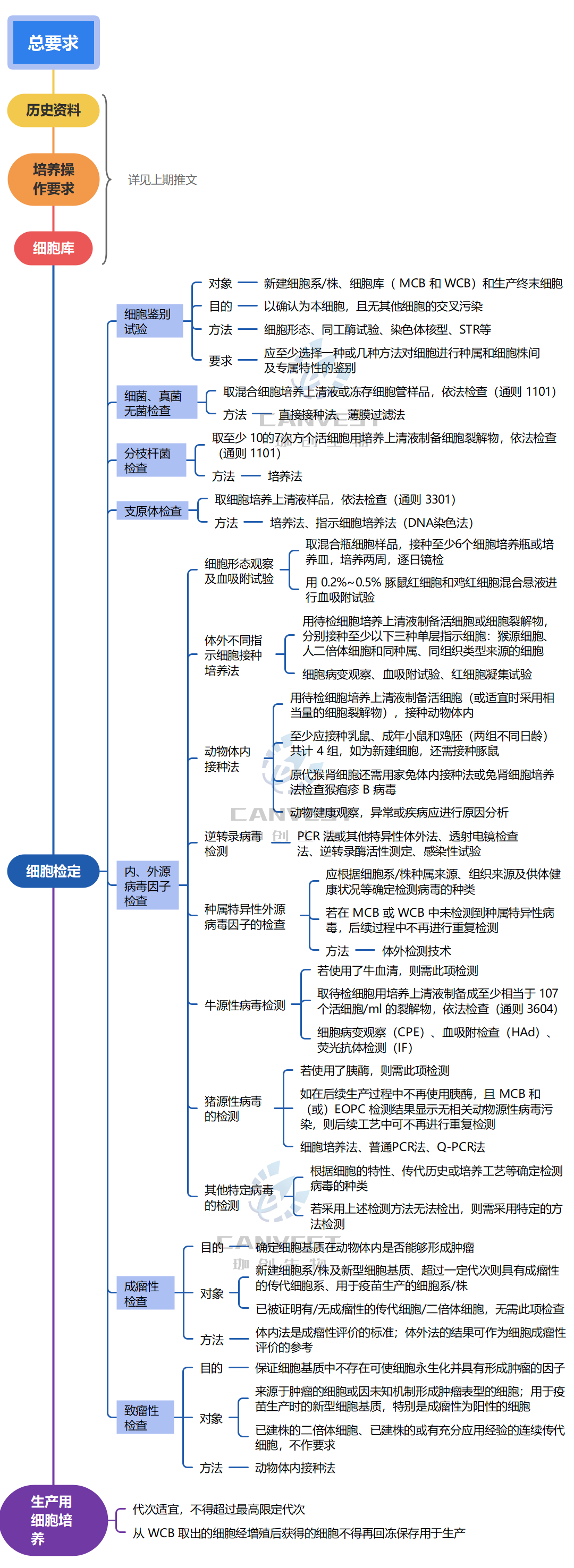
细胞检定项目表
表1、细胞检定项目基本要求▼
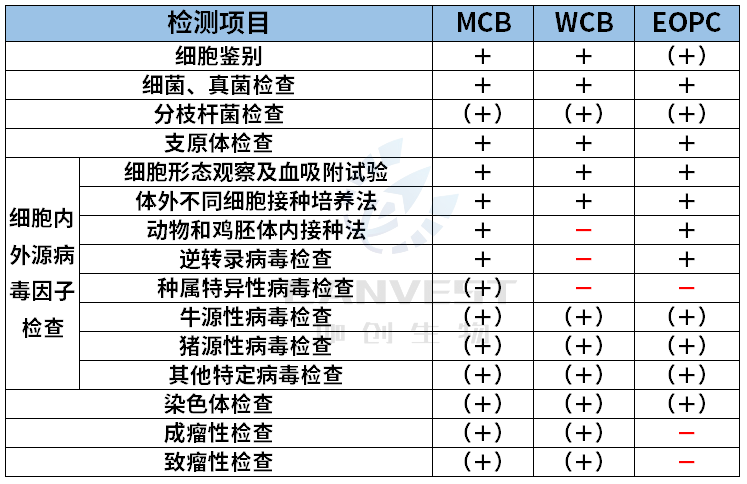
MCB:主细胞库 WCB:工作细胞库 EOPC:生产终末细胞
“+ ”为必检项目,“-”为非强制检定项目。
( + ) 表示要根据细胞特性、传代历史、培养过程等情况要求的检定项目。
表2、单克隆抗体和蛋白类产品质量检测
以CHO为例▼
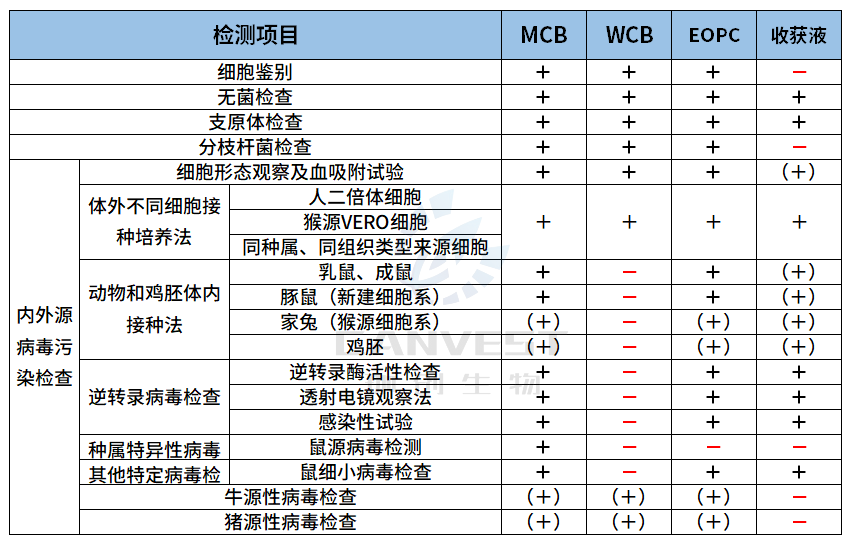
表3、细胞基因治疗产品质量检测
以293细胞为例▼
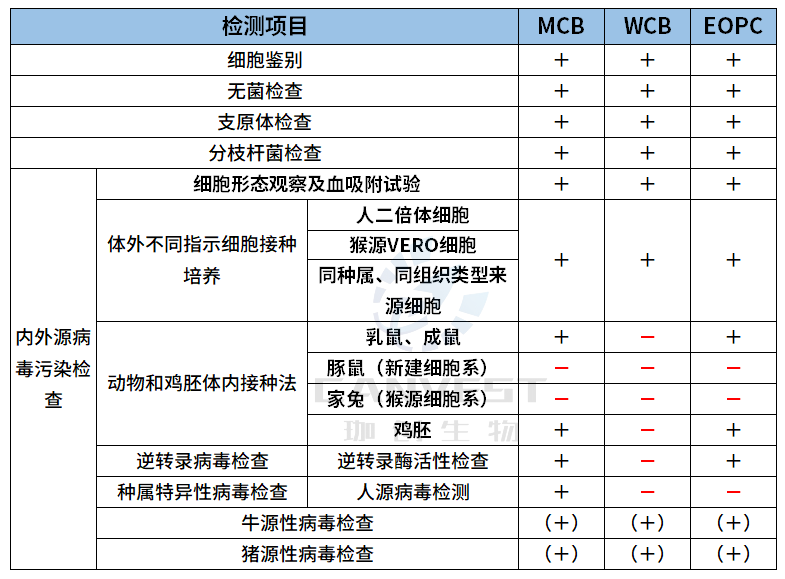
表4、干细胞类产品质量检测
以间充质干细胞(hMSCs)为例▼
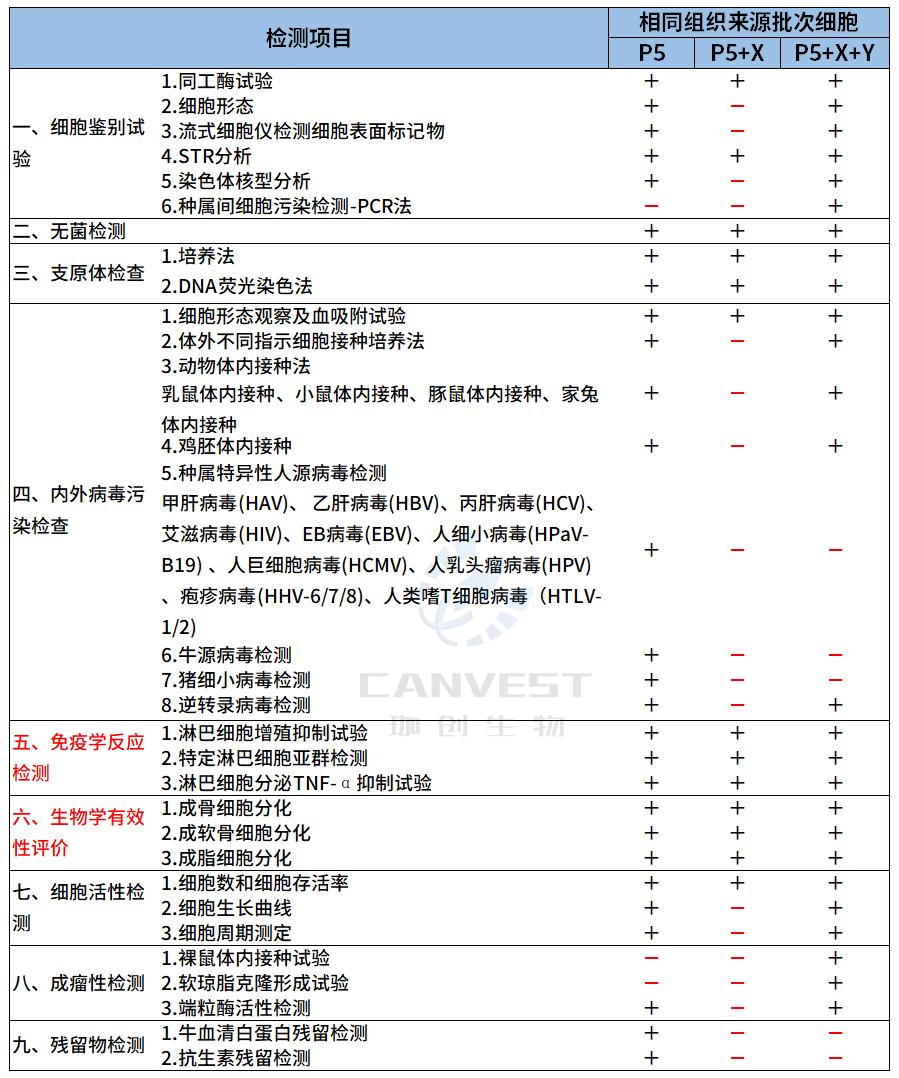
P5,P5+X,P5+X+Y分别代表初始检测代次(或临床使用代次)、初始代次后的X个扩展代次(如5个代次)、初始代次的X+Y个扩展代次(Y也可以为5个代次)。
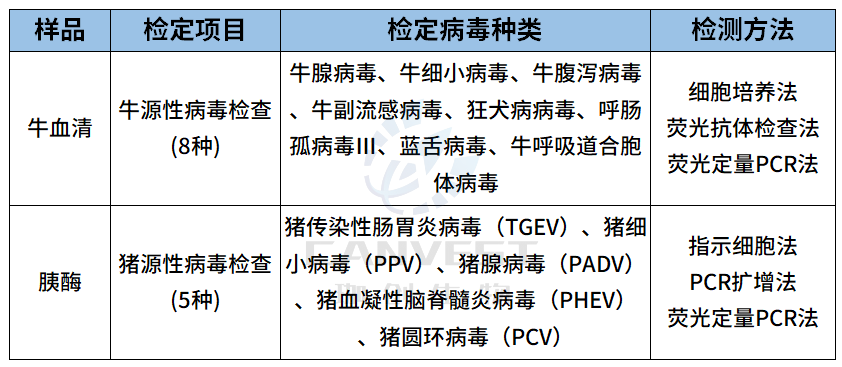
表5、原材料质量检测▼
珈创生物细胞检定相关服务
武汉珈创生物技术股份有限公司,创建于2011年,是一家集生物技术服务与研发为一体的高新技术企业,专注于为生物药品/制品的生产企业及研发机构提供各类细胞(含重组细胞、干细胞、免疫细胞等)及原辅料的质量检测、病毒清除工艺验证技术服务。
按药典要求,细胞系/株需要经过全面检定合格后,方可用于生产。
珈创生物在细胞检定领域,拥有丰富的经验积淀:其首席专家郑从义教授(原中国典型培养物保藏中心主任)自 1985 年开始从事细胞保藏/检测及细胞质量控制研究,至今已有37年,曾赴美国ATCC、荷兰真菌保藏所(CBS)、英国培养物保藏中心(NCTC)做访问学者,拥有深厚的学术积累;公司全部检测人员都经过系统、专业的岗位培训,其核心检测人员在本领域内的从业经验都在5年以上。
珈创生物应广大客户需求,已经完成参考《美国药典 USP43》、ICH指导原则及相关法规要求的技术升级,可提供涵盖细胞鉴别、纯度(无菌检查、支原体检查及内外源病毒因子检查等)和病毒清除工艺验证等符合中美欧申报要求的检测服务。