珈创生物 —— 生物技术服务与研发为一体的高新技术企业
优质高效透明
High quality, efficient and transparent
发布时间:2026-04-29 22:45 信息来源: 阅读次数: 次
2026年5月1日,《生物医学新技术临床研究和临床转化应用管理条例》(国务院令第818号,以下简称“818号令”)将正式施行。该条例的出台,意味着我国生物医学新技术从临床研究到临床转化应用,将进入更加规范、透明、可追溯的监管阶段。对于细胞治疗、基因治疗、组织工程、免疫治疗等前沿技术领域而言,818号令既是行业发展的重要机遇,也是一次合规能力的系统考验。

珈创生物结合行业关注重点,整理了以下避坑提示,助力生物医学新技术研发与临床转化规范、高效推进。
一、不要混淆“临床研究发起机构”和“临床研究机构”
818号令中,“临床研究发起机构”和“临床研究机构”是两个不同概念,不能简单等同。临床研究发起机构,是指发起生物医学新技术临床研究的机构。条例规定,临床研究发起机构应当是在我国境内依法成立的法人,并应确保拟开展临床研究的生物医学新技术已经非临床研究证明安全、有效。
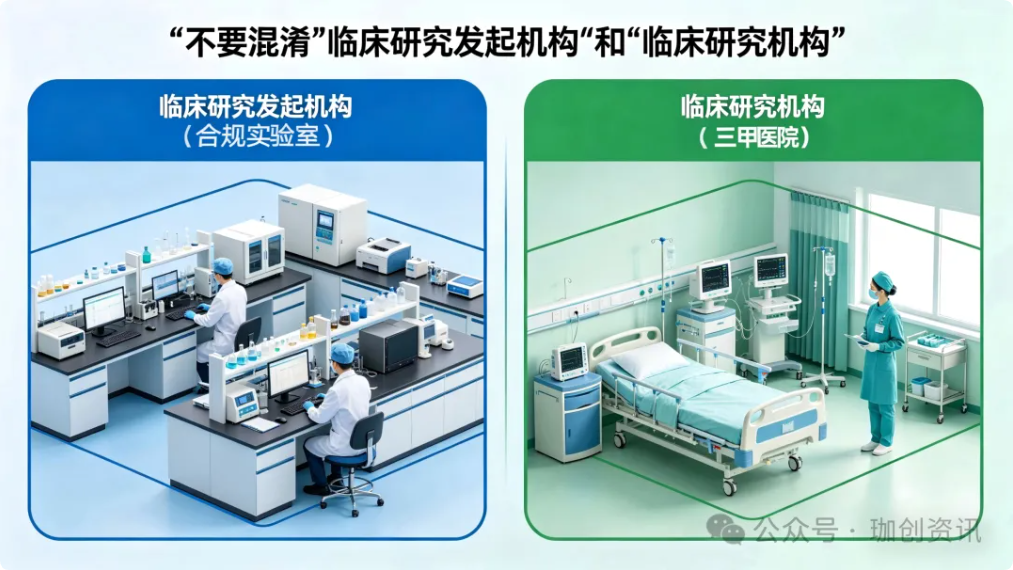
临床研究机构,则是实际实施生物医学新技术临床研究的机构。条例明确,临床研究机构应当是三级甲等医疗机构,并具备符合要求的学术委员会、伦理委员会、研究能力、质量安全管理制度以及稳定充足的研究经费来源。
也就是说,企业、科研机构等可以作为临床研究发起机构参与项目设计和推动,但真正实施临床研究的机构必须是三甲医院,三甲医院也可以自行发起生物医学新技术临床研究。
二、临床研究阶段不能向受试者收费
818号令明确规定,临床研究发起机构、临床研究机构不得向受试者收取与生物医学新技术临床研究有关的费用。这意味着,临床研究阶段不能以“治疗费”、“技术服务费”、“制备费”、“检测费”、“管理费”等名义向受试者收费。无论项目技术多么先进、制备成本多么高,只要仍处于临床研究阶段,就不能把研究成本转嫁给受试者。

真正可以按规定收费的阶段,是生物医学新技术经过临床研究后,拟转化应用于临床,并经国务院卫生健康主管部门审查批准之后。条例明确,批准临床转化应用后,符合条件的医疗机构开展临床应用,可以按照规定收取费用。
因此,企业和机构需要特别注意:临床研究不是商业化应用,备案不等于收费许可,受试者也不是付费患者。如果在临床研究阶段以各种名义收费,不仅可能引发伦理和合规问题,也可能面临退费、处罚甚至影响后续转化审批的风险。
三、不是做了质量复核,就可以直接临床备案
在研发阶段,重视样品检测、质量复核、放行检测是非常必要的。但需要明确,质量复核并不等同于临床研究备案的全部要求。
818号令规定,开展生物医学新技术临床研究前,应当依法开展实验室研究、动物实验等非临床研究;经非临床研究充分验证该技术安全、有效后方可开展临床研究。这说明,临床研究备案不是简单提交一份检测报告或质量复核报告,还需要系统开展必要的药学研究、质量研究、工艺研究、稳定性研究、非临床安全性研究、有效性研究以及风险控制方案设计等。

换句话说,质量复核是“能不能放行”的重要依据之一,但临床研究备案的重点是这项技术是否具备进入人体研究的科学基础和风险控制能力。二者层级不同,不能相互替代。
对于临床研究发起机构,尽早建立完整的研究资料体系是非常重要的,应充分考虑细胞来源、建库过程、制备工艺、关键质量属性、检测方法学、批间一致性、病毒安全性、非临床研究证据、风险预案和知情同意材料等。
四、不是所有产品都适合走“生物医学新技术临床转化”路径
818号令建立的是生物医学新技术临床研究和临床转化应用管理路径,但这并不意味着所有细胞、基因、再生医学或创新治疗产品都能纳入这一通道。
条例本身明确,为研制药品、医疗器械开展临床试验的,应当依照《药品管理法》《医疗器械监督管理条例》等法律法规执行;国务院卫生健康部门会同国务院药品监督管理部门,将根据科学技术发展制定和调整生物医学新技术与药品、医疗器械的界定指导原则。

近期公开的《生物医学新技术临床转化应用审批工作规范(征求意见稿)》进一步提出,纳入临床转化应用审批范围的技术需要已列入《生物医学新技术临床研究备案指导清单》,并满足特定条件。一类是个性化程度高,国内尚无使用同类机制原理的药品获得上市许可或者已启动确证性临床试验;另一类是用于治疗国家卫生健康委公布的《罕见病目录》收录的罕见病,且国内尚没有使用同类机制原理、针对相同适应症的药品获得上市许可或者已启动确证性临床试验。
因此,项目早期就要判断清楚:是否具有高度个性化特征、是否已有同类机制药品上市或进入确证性临床、是否属于罕见病治疗、是否已列入备案指导清单、是否涉及药品或医疗器械属性。
五、合规转化的核心,是把质量研究前移
818号令的实施,正在推动行业从“能做出来”走向“能证明、能追溯、能监管、能转化”。对于生物医学新技术而言,质量体系不应只服务于末端样品放行,而应贯穿技术开发、工艺建立、非临床研究、临床研究和转化应用全过程。
作为深耕细胞质量检验与生物安全评价领域的专业第三方技术服务机构,武汉珈创生物围绕生物医学新技术临床研究和临床转化应用过程中的关键质量环节,可为研发企业、医疗机构和科研团队提供系统化技术支持。
在早期研发和临床前阶段,珈创生物可协助开展研究用细胞的检测、细胞建库、主细胞库及工作细胞库的检测,为后续工艺开发和临床研究打好基础。

在工艺和生产阶段,珈创生物可提供工艺开发及GMP生产服务,并围绕GMP生产过程中的质量控制需求,提供原辅料检测、过程控制检测、成品质量研究、方法学开发与验证等服务,帮助研发单位建立更加完整、可追溯的质量研究体系。在病毒安全性方面,珈创生物可提供病毒清除验证、外源病毒因子检测、支原体检测、无菌检测、内毒素检测等技术服务。
在临床研究阶段,珈创生物可根据项目需求,提供临床样品快检放行、质量复核、批次检测、稳定性研究和异常结果分析等服务,提升临床样品流转效率。
对于拟进入临床转化应用的项目,珈创生物可结合检测数据、质量研究资料和风险控制要求,为研发单位和医疗机构提供质量研究体系梳理、检测策略设计和申报资料支持,助力项目迈向临床转化。
结语:818号令不是“限制创新”,而是推动创新进入规范通道
818号令的实施,不是给生物医学新技术发展踩刹车,而是为真正安全、有效的创新技术铺设更加清晰的合规路径。未来,生物医学新技术的竞争,不仅是技术先进性的竞争,更是质量体系、临床证据、伦理合规和转化能力的综合竞争。谁能更早理解政策边界,谁能更早建立完整的质量研究和风险控制体系,谁就能在临床转化过程中走得更稳、更远。

珈创生物将持续关注818号令及配套政策动态,为生物医学新技术研发和临床转化提供专业、可靠、高效的技术服务,助力创新技术在合规道路上实现真正的临床价值。